
新闻动态
奥雷巴替尼若挑战Ph+ALL成功,四项适应症开发目标有望都如期实现。
在著名血液肿瘤期刊和2023欧洲血液学协会(EHA)年会上,亚盛医药核心产品奥雷巴替尼,连续公布3项费城染色体阳性急性淋巴细胞白血病(Ph+ALL)治疗的积极数据,覆盖Ph+ALL儿童及成人、耐药及一线各类患者。
挖掘奥雷巴替尼Ph+ALL潜力
Ph+ALL在儿童中还相对少见,仅占约2%~5%。但其发病率随年龄增长而增加,Ph+ALL是成人ALL患者最常见的亚型。
一代及二代BCR-ABL1抑制剂如伊马替尼、达沙替尼等加入诱导方案,显著提升了Ph+ALL的初治效果。但该疾病控制后容易复发,目前患者5年无病生存率仅60%左右。且复发患者后续可选择的治疗手段非常有限,中枢神经系统(CNS)复发问题处理起来则更加棘手。可以说,对比其他类型白血病而言,Ph+ALL的预后较差。
而最近公布的几项研究结果,提示奥雷巴替尼有望改善Ph+ALL的治疗格局,其对于现有TKI耐药的患者仍有较好的治疗效果。
Clinical Lymphoma, Myeloma and Leukemia上发表的文章提到,中国医学科学院血液病医院儿童血液病诊疗中心主任竺晓凡和St. Jude儿童研究医院肿瘤系主任ChingHon Pui,对国内3个医疗中心2021年12月至2023年2月7名复发或其他酪氨酸激酶抑制剂(TKI)治疗不耐受的儿童Ph+ALL患者,接受奥雷巴替尼治疗后的效果进行回顾性分析。
上述两位研究者都在儿童难治性白血病治疗方面有深厚造诣。其中ChingHon Pui是儿童白血病领域全球最顶尖专家之一,他已发表论文上千篇,提出的精准治疗方案将儿童ALL的治愈率提高到90%以上,另外制定的化疗替代方案,使无数ALL患儿免受头颅放疗和由此带来的相关近、远期合并症。
这是奥雷巴替尼在Ph+ALL儿童患者中的首次临床数据披露。研究随访时间218~427天。7例患者(男5例,女2例)年龄范围为5.0~17.6岁(中位12.9岁)。肿瘤基因组检测显示5例Ph+B-ALL患者属于BCR::ABL1 p190融合;1例Ph+B-ALL患者为e1a3融合转录物;1例T-ALL患者为NUP214::ABL1融合,所有患者均无ABL激酶结构域突变。
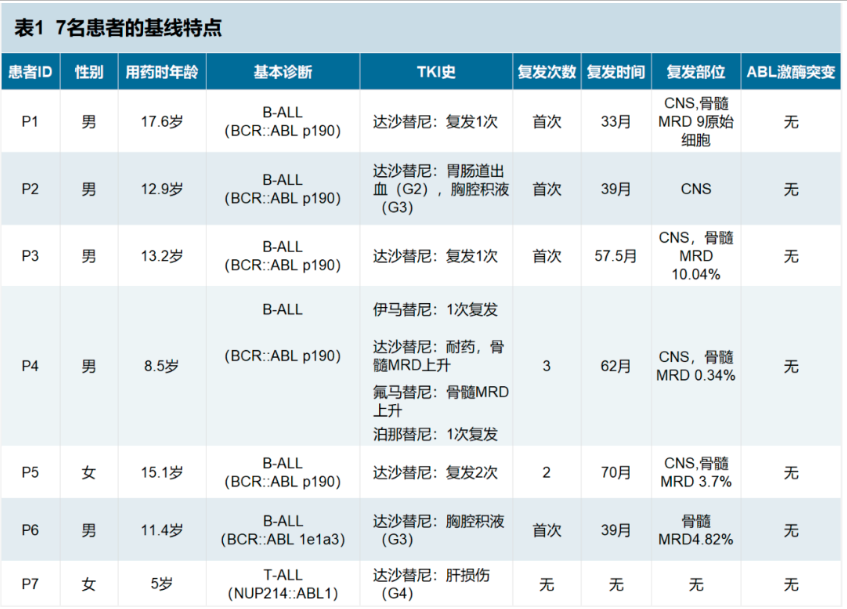
结果显示在5例可评估病例中,4例达到分子微小残留病(MRD)阴性的完全缓解,其中2例仅接受奥雷巴替尼单药治疗,即达到分子MRD阴性。
同时基线有5例患者存在CNS复发,治疗后有4例可评估患者在20~48天内达到CNS1(脑脊液样本中无原始细胞)。
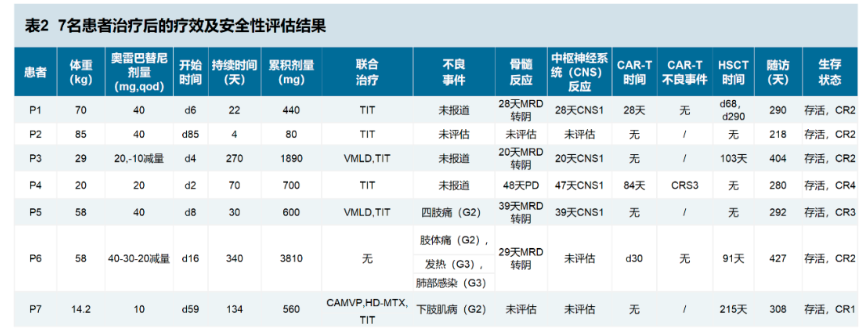
注:上表TIT:鞘内注射;CNS状态包括CNS1(脑脊液样本中无原始细胞)、CNS2 (< 5 WBC/ mm3,红细胞< 10 /mm3)和CNS3(≥5 WBC/ mm3,红细胞< 10 /mm3和/或脑神经麻痹)
本研究中奥雷巴替尼治疗的中位持续时间为70天(范围:4-340),中位累积剂量为600mg(范围:80-3810)。药物在治疗中安全性表现良好,6例安全性可评估患者仅观察到2级肢体疼痛或肌病以及3级发热,但都未因安全性问题停药。
上述研究数据初步展现,作为第三代TKI,奥雷巴替尼在复发性Ph+ALL儿童治疗中的有效性和安全性优势。此外,其显示出防治中枢神经系统白血病的潜力。
另外两项奥雷巴替尼针对成人Ph+ALL患者的研究,在EHA上进行了壁报展示。它们均为医生发起的IIT。
其中一项针对伴T315I突变复发/难治性(R/R)Ph+ALL成人患者的研究,11例分子R/R患者中,MRD阴性和完全分子生物学缓解(CMR)率分别为72.7%和63.6%;10例血液学R/R患者,MRD阴性和CMR率分别为50%和40%。
另外研究发现,具有T315I突变的患者,MRD阴性和CMR率分别为75%和62%,而没有T315I突变的患者两项均只有20%。这一点与奥雷巴替尼的作用机制对应。
另一项奥雷巴替尼联合儿科样化疗方案pdt-all-2016一线治疗Ph+ ALL的研究。其中纳入分析的13例成人患者,中位随访时间8.967个月,患者均达到CR,总有效率为100%。CMR 第14天、第30天、第60天、第90天分别为2/13(15.4%)、5/13(38.5%)、8/13(61.3%)、11/13 (84.6%) 。
Ph+ALL是奥雷巴替尼研发的第三个目标适应症,上述几项研究病例数虽少,但展现了奥雷巴替尼针对不同年龄、不同治疗阶段Ph+ALL患者的治疗潜力。
奥雷巴替尼已获批用于T315I突变的耐药CML治疗,今年还可能获批用于全部耐药CML慢性期患者;另外,琥珀酸脱氢酶缺陷型胃肠道间质瘤适应症,近日也被CDE列入突破性治疗品种名单。按目前趋势看,若挑战Ph+ALL成功,四项适应症开发目标有望都如期实现。
上文提到的竺晓凡及其团队,目前还在开展奥雷巴替尼联合亚盛医药Bcl-2抑制剂APG-2575,治疗R/R Ph+ALL儿童患者的安全性和有效性临床研究。这两个靶点产品联用,去年曾被《新英格兰医学杂志》疾病综述文章认为,是解决复发患者治疗难题的一个可能有效手段
产品线开发瞄准最新临床需求
除奥雷巴替尼外,亚盛医药的其他几个细胞凋亡通路产品,Bcl-2抑制剂APG-2575、MDM2-p53抑制剂APG-115、FAK抑制剂APG-2449近期的数据更新,也回应了当下肿瘤治疗的多个热点问题。
APG-2575在今年ASCO上公布了单药或与伊布替尼/利妥昔单抗联用,治疗华氏巨球蛋白血症(WM)的1b/2期临床研究数据。
这项研究中位观察时间虽然只有3~4个月,但其检验了APG-2575更高剂量用药的安全性。这将为其在CLL/SLL/AML适应症外,创造更多的研究拓展机会。
该研究分成三个亚组进行,使用最大剂量为1200mg,是维奈克拉400mg用药剂量的3倍,但研究中受试者仍表现出良好的安全性和耐受性。目前APG-2575尚未达到最大耐受剂量。B组在递增至1200mg时,观察到1例剂量限制毒性(DLT,3级临床TLS),考虑主要与自身既往存在的肾功能损害相关。未观察到APG-2575与伊布替尼有潜在药物-药物相互作用(DDI)。
在疗效方面,A组14位既往接受过BTK抑制剂治疗的患者,接受APG-2575单药治疗,ORR为50%;B组24位初治患者,接受APG-2575联合伊布替尼治疗,ORR为100%;C组8位未接受过BTK治疗的复发/耐药患者,接受APG-2575联合利妥昔单抗治疗,ORR为62.5%。其中B组两例患者达到非常好的部分缓解(VGPR)。
亚盛方面此前提到,Bcl-2抑制剂用于WM或者多发性骨髓瘤(MM)治疗,均需要更高的用药剂量才能起效。目前APG-2575已在MM、WM、复发/难治性非霍奇金淋巴瘤等疾病上开展研究,其中包括维奈克拉因安全性问题折戟的适应症。
APG-115公布的数据,则进一步夯实了其用于肿瘤免疫耐药患者的治疗效果。APG-115与帕博利珠单抗联合,用于PD-1抑制剂耐药的黑色素瘤治疗,这项研究数据近几年持续更新。
其中研究包含的皮肤黑色素瘤队列,2021年ASCO上公布的15例患者,有1例CR(已确认)和3例PR(2例确认+1例未确认);2022年ASCO上的20例患者,有2例CR和2例PR,ORR为20%;2023年ASCO患者增加到31例,26例疗效可评估患者,有2例CR和4例PR,ORR为23.1%。
这项研究随着多年数据积累和受试者数量增加,ORR都保持相对稳定,说明APG-115有克服肿瘤免疫耐药的潜力。
另一款处于早期临床阶段的产品APG-2449,其原先被作为三代ALK抑制剂开发,赛道较为拥挤。但随着临床研究推进,数据分析发现APG-2449对FAK磷酸化有明显抑制作用。
今年ASCO公布的数据,接受APG-2449治疗的28例二代ALK抑制剂耐药的NSCLC 患者,有8例患者获得PR(8/28; 28.6%)。研究对患者FAK水平进行分析结,发现获得PR的患者,FAK水平降低比SD或者病情进展的患者更明显。其推断APG-2449可以抑制FAK磷酸化,而基线肿瘤组织磷酸化FAK表达较高的患者,可能获得更佳的临床反应。
这意味着APG-2449可能为二代ALK抑制剂耐药的NSCLC患者,提供克服耐药的新治疗策略,同时有望解决更广泛的肿瘤耐药复发问题。FAK被认为在肿瘤细胞凋亡中起重要作用,是肿瘤耐药及转移的帮凶。